LEVONORGESTREL ETHINYLESTRADIOL
Les gammes de produits
LEVONO/ETHINY BIOGARAN 30microgrammes/150microgr cp
Remboursable
Sur prescription seulement
Forme :
Comprimé enrobé
Catégories :
Contraception et interruption de grossesse, Contraception hormonale, Estroprogestatifs combinés, Minidosés : = < 0,04 mg d'éthinylestradiol, Monophasiques, Lévonorgestrel + Ethinylestradiol, Lévonorgestrel + Ethinylestradiol : prise sur 21 jours
Principes actifs :
Lévonorgestrel, Ethinylestradiol
Posologie pour LEVONO/ETHINY BIOGARAN 30microgrammes/150microgr cp
Indications
Contraception orale
Posologie
Adulte Femme . en âge de procréer. Contraception orale (implicite)
1 comprimé par jour au même moment de la journée à prendre régulièrement et sans oubli pendant 21 jours.
Puis arrêt pendant 7 jours.
Administration
Voie orale
Recommandations patient
CONSULTER
IMMÉDIATEMENT LE MÉDECIN en cas :
- De
gonflement de la jambe ou du pied, accompagnée d'une douleur ou sensibilité,
ressentie qu'en position debout ou lors de la marche ; chaleur, changement
de couleur de la partie affectée.
- D'un
essoufflement ou d'une respiration rapide, d'apparition soudaine et
inexpliquée ; toux sans cause apparente avec parfois des crachats de
sang ; douleurs aiguës dans la poitrine, qui peut s'accentuer lors de
respirations profondes ; étourdissements ou sensations vertigineuses
sévères ; battements de cœur rapides ou irréguliers ; douleurs intenses
au niveau de l'estomac.
- De
perte immédiate de la vision ou vision trouble sans douleur le plus souvent
dans un seul œil.
- De
sensation de lourdeur, gêne, sensation d'oppression ou d'encombrement de la
poitrine, bras ou sous le sternum, du haut du corps irradiant vers le dos, la
mâchoire, la gorge, le bras et l'estomac ; faiblesse, anxiété,
essoufflements, transpiration, sensations vertigineuses, nausées, vomissements.
- D'apparition
soudaine d'une faiblesse ou d'un engourdissement au niveau du visage, d'un bras
ou d'une jambe, en particulier d'un côté du corps ; confusion, difficulté
à comprendre ou parler ; difficulté à marcher, perte d'équilibre ou de
coordination ; maux de tête soudains, sévères ou prolongés sans cause
connue ; perte de connaissance avec ou sans crise convulsives.
-
De réaction allergique grave dont les symptômes peuvent être : respiration
sifflante soudaine, difficulté respiratoire ou sensations vertigineuses,
gonflement des paupières, du visage, des lèvres ou de la gorge, éruption
cutanée, urticaire.
-
De vomissements, diarrhée (qui peut être sanguinolente), fièvre, sensation de
faiblesse, diminution de la production d'urine.
- De pancréatite caractérisée par une douleur grave dans le haut du ventre,
pouvant s'étendre dans le dos.
- D'éruption cutanée avec des taches roses ou rouges, particulièrement sur la
paume des mains et la plante des pieds, avec éventuellement formation de
cloques et pouvant s'accompagner d'ulcères au niveau de la bouche, des yeux ou
des organes génitaux, et de fièvre.
CONSULTER
LE MÉDECIN en cas de :
- Spottings
persistant plus de 7 jours.
- Changement
d'humeur ou symptômes dépressifs.
Il pourra être nécessaire d'INTERROMPRE LE
TRAITEMENT, en cas :
- D'opération
chirurgicale.
- D'alitement
pendant une période prolongée en raison d'une blessure, maladie ou
immobilisation de la jambe.
ÉVITER toute exposition directe au soleil ou rayons UV en cas d'antécédent ou
de survenue de taches brun doré sur le visage, aussi appelée masque de
grossesse.
NE PAS CONSOMMER de millepertuis (Hypericum perforatum) pendant le traitement
(possibilité de diminuer l'efficacité contraceptive du médicament).
INFORMER LE LABORATOIRE de la prise
de ce médicament en cas d'examen sanguin.
Contre-indications pour LEVONO/ETHINY BIOGARAN 30microgrammes/150microgr cp
- Thrombo-embolie veineuse
- Antécédent thrombo-embolique veineux
- Antécédent d'embolie pulmonaire
- Risque thromboembolique
- Résistance à la protéine C activée
- Déficit en antithrombine III
- Carence en protéine C
- Carence en protéine S
- Prédisposition aux thrombo-embolies
- Intervention chirurgicale majeure
- Immobilisation prolongée
- Thrombo-embolie artérielle
- Infarctus du myocarde
- Prodrome d'accident thrombo-embolique artériel
- Maladie cérébrovasculaire
- Accident vasculaire cérébral
- Antécédent d'AVC
- Hyperhomocystéinémie
- Présence d'anticorps antiphospholipides
- Antécédent de migraine avec signes neurologiques focalisés
- Diabète avec atteinte vasculaire
- Hypertension artérielle sévère
- Dyslipoprotéinémie sévère
- Pancréatite
- Antécédent de pancréatite associée à une hypertriglycéridémie sévère
- Affection hépatique sévère ou antécédent en l'absence de normalisation des tests fonctionnels hépatiques
- Tumeur hépatique évolutive
- Tumeur hépatique ancienne
- Tumeur hormonodépendante (de la femme)
- Saignement vaginal non diagnostiqué
- Sujet de sexe masculin
- Patient de moins de 12 ans
- Grossesse
- Sujet de sexe féminin de 12 à 15 ans
- Intolérance au lactose
- Malabsorption du glucose-galactose
- Allaitement
Effets indésirables pour LEVONO/ETHINY BIOGARAN 30microgrammes/150microgr cp
Niveau d’apparition des effets indésirables
Peu fréquent
Alopécie
Chloasma
Hirsutisme
Hypertension artérielle
Diminution de l'appétit
Elévation de la pression artérielle
Crampe abdominale
Augmentation de l'appétit
Ballonnement abdominal
Rash cutané
Modification des lipides plasmatiques
Rare
Thrombo-embolie veineuse
Réaction anaphylactique
Trouble respiratoire
Angio-oedème
Erythème noueux
Ictère cholestatique
Intolérance au glucose
Thrombo-embolie artérielle
Irritation par les lentilles de contact
Trouble circulatoire
Très rare
Cholestase
Lithiase biliaire
Névrite optique
Pancréatite
Urticaire allergique
Erythème polymorphe
Syndrome hémolytique urémique
Colite ischémique
Carcinome hépatocellulaire
Exacerbation d'une chorée
Exacerbation d'une porphyrie
Exacerbation d'un lupus érythémateux disséminé
Réduction des taux sériques de folates
Tumeur hépatique bénigne
Exacerbation des varices
Inconnu
Accident vasculaire cérébral
Candidose vaginale
Hépatite
Hypertriglycéridémie
Infarctus du myocarde
Lupus érythémateux disséminé
Maladie de Crohn
Otosclérose
Phlébite
Porphyrie
Prurit de cholestase
Dépression
Embolie pulmonaire
Modification de la libido
Spotting
Colite ulcéreuse
Adénome hépatique
Accident ischémique transitoire
Fonction hépatique anormale
Chorée de Sydenham
Aggravation de l'épilepsie
Aggravation de lithiase biliaire
Aggravation de la dépression
Atteinte hépatocellulaire
Aggravation de maladie de Crohn
Aggravation d'angioedème
Angioedème héréditaire
Hyperplasie nodulaire hépatique focale
Exacerbation d'une chorée de Sydenham
Exacerbation de rectocolite hémorragique
Aggravation de l'otosclérose
Les effets indésirables suivants ont été observés pendant le traitement par contraceptifs estroprogestatifs oraux :
Pour les effets indésirables graves, tels que les accidents thromboemboliques veineux et artériels, les cancers du col de l'utérus, les cancers du sein et les tumeurs hépatiques malignes,voir rubrique Mises en garde et précautions d'emploi.
Une augmentation du risque d'événement thrombotique et thrombo-embolique artériel et veineux, incluant l'infarctus du myocarde, l'AVC, les accidents ischémiques transitoires, la thrombose veineuse et l'embolie pulmonaire, a été observée chez les femmes utilisant des CHC ; ceci est abordé plus en détails en rubrique Mises en garde et précautions d'emploi.
Les oestrogènes exogènes peuvent déclencher ou aggraver les symptômes d'un angio-oedème héréditaire ou acquis.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence Nationale de Sécurité du Médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : signalement.social-sante.gouv.fr.
Voir plus
Grossesse et allaitement pour le LEVONO/ETHINY BIOGARAN 30microgrammes/150microgr cp
Grossesse
LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN n'est pas indiqué pendant la grossesse. En cas de découverte d'une grossesse sous ce médicament, son utilisation doit immédiatement être interrompue.
De nombreuses études épidémiologiques n'ont pas révélé d'augmentation du risque d'anomalies congénitales chez les enfants nés de femmes ayant utilisé un contraceptif oral avant la grossesse.
Aucun effet tératogène n'a été observé lorsqu'un contraceptif oral combiné a été pris par erreur en début de grossesse.
L'augmentation du risque de TEV en période post-partum doit être prise en compte lors de la reprise de LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN (voir rubriques Posologie et mode d'administration et Mises en garde et précautions d'emploi).
Allaitement
En cas d'allaitement, l'utilisation de ce médicament est déconseillée en raison du passage des estroprogestatifs dans le lait maternel.
Si la femme désire allaiter, un autre moyen de contraception doit être proposé.
Mise en garde pour LEVONO/ETHINY BIOGARAN 30microgrammes/150microgr cp
Mise en garde
Si la patiente présente l'un des troubles ou l'un des facteurs de risque mentionnés ci-dessous, la pertinence du traitement par LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN doit être discutée avec elle.
En cas d'aggravation ou de survenue de l'un de ces troubles ou facteurs de risque, la nécessité d'interrompre l'utilisation de LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN doit être discutée entre le médecin et la patiente.
LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN et Thrombose
Risque de thrombo-embolie veineuse (TEV)
Le risque de TEV est augmenté chez les femmes qui utilisent un contraceptif hormonal combiné (CHC) en comparaison aux femmes qui n'en utilisent pas. Les CHC contenant du lévonorgestrel, du norgestimate ou de la noréthistérone sont associés au risque de TEV le plus faible. La décision d'utiliser LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN doit être prise uniquement après concertation avec la patiente afin de s'assurer qu'elle comprend le risque de TEV associé à LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN, l'influence de ses facteurs de risque actuels sur ce risque et le fait que le risque de TEV est maximal pendant la première année d'utilisation. Certaines données indiquent également une augmentation du risque lors de la reprise d'un CHC après une interruption de 4 semaines ou plus.
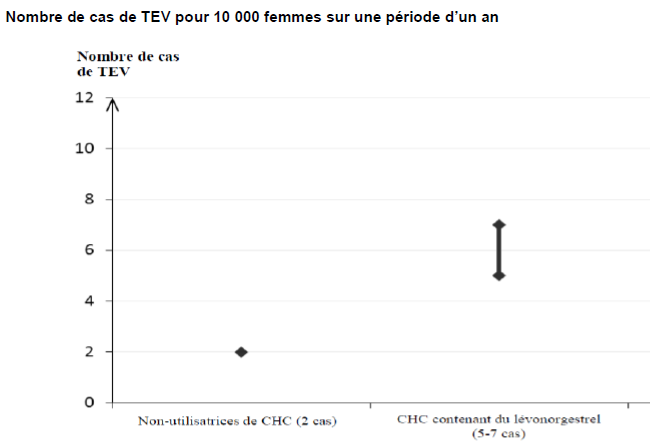
Parmi les femmes qui n'utilisent pas de CHC et qui ne sont pas enceintes, environ 2 sur 10 000 développeront une TEV sur une période d'un an. Cependant, chez une femme donnée, le risque peut être considérablement plus élevé, selon les facteurs de risque qu'elle présente (voir ci-dessous).
On estime que sur 10 000 femmes qui utilisent un CHC contenant du lévonorgestrel, 61 développeront une TEV sur une période d'un an.
1 Point central de l'intervalle de 5-7 pour 10 000 années-femmes sur la base d'un risque relatif, pour les CHC contenant du lévonorgestrel par rapport à la non utilisation d'un CHC, d'environ 2,3 à 3,6.
Ce nombre de TEV par année est inférieur à celui attendu pendant la grossesse ou en période post‑partum.
La TEV peut être fatale dans 1 à 2 % des cas.
De façon extrêmement rare, des cas de thrombose ont été signalés chez des utilisatrices de CHC dans d'autres vaisseaux sanguins, p. ex. les veines et artères hépatiques, mésentériques, rénales ou rétiniennes.
Facteurs de risque de TEV
Le risque de complications thrombo-emboliques veineuses chez les utilisatrices de CHC peut être considérablement accru si d'autres facteurs de risque sont présents, en particulier si ceux-ci sont multiples (voir le tableau ci-dessous).
LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN est contre-indiqué chez les femmes présentant de multiples facteurs de risque, ceux-ci les exposant à un risque élevé de thrombose veineuse (voir rubrique Contre-indications). Lorsqu'une femme présente plus d'un facteur de risque, il est possible que l'augmentation du risque soit supérieure à la somme des risques associés à chaque facteur pris individuellement - dans ce cas, le risque global de TEV doit être pris en compte. Si le rapport bénéfice/risque est jugé défavorable, le CHC ne doit pas être prescrit (voir rubrique Contre-indications).
Tableau : Facteurs de risque de TEV
| Facteur de risque | Commentaire |
| Obésité (indice de masse corporelle supérieur à 30 kg/m²) | L'élévation de l'IMC augmente considérablement le risque. Ceci est particulièrement important à prendre en compte si d'autres facteurs de risque sont présents. |
| Immobilisation prolongée, intervention chirurgicale majeure, toute intervention chirurgicale sur les jambes ou le bassin, neurochirurgie ou traumatisme majeur Remarque : l'immobilisation temporaire, y compris les trajets aériens > 4 heures, peut également constituer un facteur de risque de TEV, en particulier chez les femmes présentant d'autres facteurs de risque | Dans ces situations, il est conseillé de suspendre l'utilisation de la pilule (au moins quatre semaines à l'avance en cas de chirurgie programmée) et de ne reprendre le CHC que deux semaines au moins après la complète remobilisation. Une autre méthode de contraception doit être utilisée afin d'éviter une grossesse non désirée. Un traitement anti-thrombotique devra être envisagé si LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN n'a pas été interrompu à l'avance. |
| Antécédents familiaux (thrombo‑embolie veineuse survenue dans la fratrie ou chez un parent, en particulier à un âge relativement jeune, c.-à-d. avant 50 ans) | En cas de prédisposition héréditaire suspectée, la femme devra être adressée à un spécialiste pour avis avant toute décision concernant l'utilisation de CHC. |
| Autres affections médicales associées à la TEV | Cancer, lupus érythémateux disséminé, syndrome hémolytique et urémique, maladies inflammatoires chroniques intestinales (maladie de Crohn ou rectocolite hémorragique) et drépanocytose. |
| Âge | En particulier au-delà de 35 ans. |
Il n'existe aucun consensus quant au rôle éventuel joué par les varices et les thrombophlébites superficielles dans l'apparition ou la progression d'une thrombose veineuse.
L'augmentation du risque de thrombo-embolie pendant la grossesse, et en particulier pendant les 6 semaines de la période puerpérale, doit être prise en compte (pour des informations concernant « Grossesse et allaitement », voir rubrique Fertilité, grossesse et allaitement).
Symptômes de TEV (thrombose veineuse profonde et embolie pulmonaire)
Les femmes doivent être informées qu'en cas d'apparition de ces symptômes, elles doivent consulter un médecin en urgence et lui indiquer qu'elles utilisent un CHC.
Les symptômes de la thrombose veineuse profonde (TVP) peuvent inclure :
· gonflement unilatéral d'une jambe et/ou d'un pied ou le long d'une veine de la jambe ;
· douleur ou sensibilité dans une jambe, pouvant n'être ressentie qu'en position debout ou lors de la marche ;
· sensation de chaleur, rougeur ou changement de la coloration cutanée de la jambe affectée.
Les symptômes de l'embolie pulmonaire (EP) peuvent inclure :
· apparition soudaine et inexpliquée d'un essoufflement ou d'une accélération de la respiration ;
· toux soudaine, pouvant être associée à une hémoptysie ;
· douleur thoracique aiguë ;
· étourdissements ou sensations vertigineuses sévères ;
· battements cardiaques rapides ou irréguliers.
Certains de ces symptômes (p. ex. « essoufflement », « toux ») ne sont pas spécifiques et peuvent être interprétés à tort comme des signes d'événements plus fréquents ou moins sévères (infections respiratoires, p. ex.).
Les autres signes d'une occlusion vasculaire peuvent inclure : douleur soudaine, gonflement et coloration légèrement bleutée d'une extrémité.
Si l'occlusion se produit dans l'oeil, les symptômes peuvent débuter sous la forme d'une vision trouble indolore pouvant évoluer vers une perte de la vision. Dans certains cas, la perte de la vision peut survenir presque immédiatement.
Risque de thrombo-embolie artérielle (TEA)
Des études épidémiologiques ont montré une association entre l'utilisation de CHC et l'augmentation du risque de thrombo-embolie artérielle (infarctus du myocarde) ou d'accident cérébrovasculaire (p. ex. accident ischémique transitoire, AVC). Les événements thrombo-emboliques artériels peuvent être fatals.
Facteurs de risque de TEA
Le risque de complications thrombo-emboliques artérielles ou d'accident cérébrovasculaire chez les utilisatrices de CHC augmente avec la présence de facteurs de risque (voir le tableau). LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN est contre-indiqué chez les femmes présentant un facteur de risque sévère ou de multiples facteurs de risque de TEA qui les exposent à un risque élevé de thrombose artérielle (voir rubrique Contre-indications). Lorsqu'une femme présente plus d'un facteur de risque, il est possible que l'augmentation du risque soit supérieure à la somme des risques associés à chaque facteur pris individuellement - dans ce cas, le risque global doit être pris en compte. Si le rapport bénéfice/risque est jugé défavorable, le CHC ne doit pas être prescrit (voir rubrique Contre-indications).
Tableau : Facteurs de risque de TEA
| Facteur de risque | Commentaire |
| Âge | En particulier au-delà de 35 ans. |
| Tabagisme | Il doit être conseillé aux femmes de ne pas fumer si elles souhaitent utiliser un CHC. Il doit être fortement conseillé aux femmes de plus de 35 ans qui continuent de fumer d'utiliser une méthode de contraception différente. |
| Hypertension artérielle | |
| Obésité (indice de masse corporelle supérieur à 30 kg/m2) | L'élévation de l'IMC augmente considérablement le risque. Ceci est particulièrement important à prendre en compte chez les femmes présentant d'autres facteurs de risque. |
| Antécédents familiaux (thrombo‑embolie artérielle survenue dans la fratrie ou chez un parent, en particulier à un âge relativement jeune, c.-à-d. avant 50 ans) | En cas de prédisposition héréditaire suspectée, la femme devra être adressée à un spécialiste pour avis avant toute décision concernant l'utilisation de CHC. |
| Migraine | L'accroissement de la fréquence ou de la sévérité des migraines lors de l'utilisation d'un CHC (qui peut être le prodrome d'un événement cérébrovasculaire) peut constituer un motif d'arrêt immédiat du CHC. |
| Autres affections médicales associées à des événements indésirables vasculaires | Diabète, hyperhomocystéinémie, valvulopathie cardiaque et fibrillation auriculaire, dyslipoprotéinémie et lupus érythémateux disséminé. |
Symptômes de TEA
Les femmes doivent être informées qu'en cas d'apparition de ces symptômes, elles doivent consulter un médecin en urgence et lui indiquer qu'elles utilisent un CHC.
Les symptômes d'un accident cérébrovasculaire peuvent inclure :
· apparition soudaine d'un engourdissement ou d'une faiblesse du visage, d'un bras ou d'une jambe, en particulier d'un côté du corps ;
· apparition soudaine de difficultés à marcher, de sensations vertigineuses, d'une perte d'équilibre ou de coordination ;
· apparition soudaine d'une confusion, de difficultés à parler ou à comprendre ;
· apparition soudaine de difficultés à voir d'un oeil ou des deux yeux ;
· céphalée soudaine, sévère ou prolongée, sans cause connue ;
· perte de conscience ou évanouissement avec ou sans crise convulsive.
Des symptômes temporaires suggèrent qu'il s'agit d'un accident ischémique transitoire (AIT).
Les symptômes de l'infarctus du myocarde (IM) peuvent inclure :
· douleur, gêne, pression, lourdeur, sensation d'oppression ou d'encombrement dans la poitrine, le bras ou sous le sternum ;
· sensation de gêne irradiant vers le dos, la mâchoire, la gorge, le bras, l'estomac ;
· sensation d'encombrement, d'indigestion ou de suffocation ;
· transpiration, nausées, vomissements ou sensations vertigineuses ;
· faiblesse, anxiété ou essoufflement extrêmes ;
· battements cardiaques rapides ou irréguliers.
LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN et Tumeurs
Certaines études épidémiologiques suggèrent que les CHC pourraient être associés à une augmentation du risque de cancer du col de l'utérus chez les utilisatrices de CHC au long cours (> 5 ans). Il n'est cependant pas établi si ces pathologies sont dues à d'autres facteurs comme le comportement sexuel et le papillomavirus virus humain (HPV).
Une méta-analyse de 54 études épidémiologiques a conclu qu'il existe une légère augmentation du risque relatif (RR = 1,24) de cancer du sein chez les femmes sous contraception orale. Cette majoration du risque disparaît progressivement au cours des 10 ans qui suivent l'arrêt du CHC.
Le cancer du sein étant rare chez les femmes de moins de 40 ans, le nombre plus élevé de cancers diagnostiqués chez les utilisatrices habituelles ou nouvelles utilisatrices de CHC reste faible par rapport au risque global de cancer du sein.
Ces études ne permettent pas d'établir une relation de causalité. Il est possible que, chez les utilisatrices de CHC, cette augmentation du risque soit due à un diagnostic plus précoce du cancer du sein, aux effets biologiques de cette contraception ou à l'association des deux. Les cancers du sein diagnostiqués chez les utilisatrices ont tendance à être moins évolués cliniquement par rapport à ceux diagnostiqués chez des femmes n'en ayant jamais utilisé.
Dans de rares cas, des tumeurs bénignes du foie (par exemple : adénome hépatique, hyperplasie nodulaire focale), et dans de plus rares cas encore, des tumeurs malignes du foie ont été rapportées chez des utilisatrices de CHC.
Dans des cas isolés, ces tumeurs ont conduit à des hémorragies intra-abdominales mettant en jeu le pronostic vital. Chez les femmes sous CHC, la survenue de douleurs de la partie supérieure de l'abdomen, d'augmentation du volume du foie ou de signes d'hémorragie intra-abdominale doit faire évoquer une tumeur hépatique.
L'utilisation de CHC plus fortement dosés (50 microgrammes d'éthinylestradiol) diminue le risque de cancer de l'endomètre et de l'ovaire. Ceci demande à être confirmé avec les CHC plus faiblement dosés.
Autres pathologies
Hypertriglycéridémie
Chez les femmes atteintes d'hypertriglycéridémie ou ayant des antécédents familiaux d'hypertriglycéridémie, un risque accru de pancréatite peut survenir en cas d'utilisation d'un CHC.
Hypertension artérielle
Une augmentation modérée de la pression artérielle a été observée chez de nombreuses femmes sous CHC mais elle était rarement cliniquement significative. Une interruption immédiate du CHC n'est justifiée que dans ces rares cas.
La persistance de chiffres tensionnels élevés ou le non contrôle des chiffres tensionnels par un traitement antihypertenseur chez une femme hypertendue prenant un CHC doit faire interrompre celle-ci.
Le CHC pourra éventuellement être repris après normalisation des chiffres tensionnels par un traitement antihypertenseur.
Affections hépatiques
La survenue d'anomalies hépatiques aiguës ou chroniques peut nécessiter l'arrêt du CHC jusqu'à la normalisation des paramètres hépatiques.
Angio-oedème
Les oestrogènes exogènes peuvent déclencher ou aggraver les symptômes d'un angio-oedème héréditaire ou acquis.
Intolérance au glucose/Diabète
Les CHC peuvent avoir un effet sur la résistance périphérique à l'insuline et la tolérance au glucose ; il n'est cependant pas obligatoire de modifier le traitement chez des diabétiques utilisant un CHC faiblement dosé (contenant moins de 0,05 mg d'éthinylestradiol). Les femmes diabétiques doivent cependant être étroitement surveillées, en particulier lors de l'instauration d'un CHC.
Autres
La récidive d'un ictère cholestatique et/ou d'un prurit liés à une cholestase survenue au cours d'une grossesse précédente ou de la prise antérieure d'hormones stéroïdiennes doit faire arrêter le CHC.
La survenue ou l'aggravation des pathologies suivantes a été observée au cours de la grossesse ou chez des femmes prenant des CHC, bien que la responsabilité des CHC n'ait pu être établie : ictère et/ou prurit dû à une cholestase, lithiase biliaire, porphyrie, lupus érythémateux disséminé, syndrome hémolytico-urémique, chorée de Sydenham, herpès gravidique, hypoacousie par otosclérose.
Des cas d'aggravations de dépression endogène, d'épilepsie, de maladie de Crohn et de rectocolite hémorragique ont été observés sous CHC.
L'état dépressif et la dépression sont des effets indésirables bien connus liés à l'utilisation de contraceptifs hormonaux (voir rubrique Effets indésirables). La dépression peut être grave et constitue un facteur de risque bien connu de comportement suicidaire et de suicide. Il convient de conseiller aux femmes de contacter leur médecin en cas de changements d'humeur et de symptômes dépressifs, y compris peu de temps après le début du traitement.
Un chloasma peut survenir, en particulier chez les femmes ayant des antécédents de chloasma gravidique. Les femmes ayant une prédisposition au chloasma sous CHC doivent éviter de s'exposer au soleil ou aux rayons ultra-violets.
Une attention particulière devra être portée aux patientes ayant une hyperprolactinémie.
Elévations des ALAT
Lors d'études cliniques incluant des patients traités pour des infections par le virus de l'hépatite C (VHC) par des médicaments contenant l'association ombitasvir/paritaprévir/ritonavir et le dasabuvir avec ou sans ribavirine, les élévations des transaminases (ALAT) supérieures à 5 fois la limite supérieure de la normale (LSN) étaient significativement plus fréquentes chez les femmes utilisant des médicaments contenant de l'éthinylestradiol tels que les contraceptifs hormonaux combinés (CHC). Des élévations des ALAT ont également été observées avec des médicaments antiviraux contre l'hépatite C, contenant du glécaprévir/pibrentasvir et du sofosbuvir/velpatasvir/voxilaprévir (voir rubriques Contre-indications et Interactions avec d'autres médicaments et autres formes d'interactions).
Consultation/examen médical
Avant l'instauration ou la reprise d'un traitement par LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN, une recherche complète des antécédents médicaux (y compris les antécédents familiaux) doit être effectuée et la présence d'une grossesse doit être exclue. La pression artérielle doit être mesurée et un examen physique doit être réalisé, en ayant à l'esprit les contre-indications (voir rubrique Contre-indications) et les mises en garde (voir rubrique Mises en garde et précautions d'emploi). Il est important d'attirer l'attention des patientes sur les informations relatives à la thrombose veineuse et artérielle, y compris le risque associé à LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN comparé à celui associé aux autres CHC, les symptômes de la TEV et de la TEA, les facteurs de risque connus et la conduite à tenir en cas de suspicion de thrombose.
Il doit également être indiqué aux patientes de lire attentivement la notice et de suivre les conseils fournis. La fréquence et la nature des examens doivent être définies sur la base des recommandations en vigueur et adaptées à chaque patiente.
Les patientes doivent être averties que les contraceptifs hormonaux ne protègent pas contre l'infection par le VIH (SIDA) et les autres maladies sexuellement transmissibles.
Examens biologiques
L'utilisation de contraceptifs hormonaux peut modifier les résultats de certains examens biologiques tels que : les tests fonctionnels hépatiques, thyroïdiens, surrénaliens et rénaux, le taux plasmatique des protéines (porteuses) comme la corticosteroid-binding globulin (CBG) et des fractions lipidiques/lipoprotéiniques, les paramètres du métabolisme glucidique, les paramètres de la coagulation et de la fibrinolyse. Les modifications restent en général dans les limites de la normale.
Diminution de l'efficacité
L'efficacité des CHC peut être réduite en cas d'oubli de comprimés actifs (voir rubrique Posologie et mode d'administration), de troubles gastro-intestinaux (voir rubrique Posologie et mode d'administration) ou de prise concomitante d'autres médicaments (voir rubrique Interactions avec d'autres médicaments et autres formes d'interactions).
Troubles du cycle
Des saignements irréguliers (« spottings » ou métrorragies) peuvent survenir sous contraceptifs oraux, en particulier au cours des premiers mois. Ces saignements irréguliers seront considérés comme significatifs s'ils persistent après environ 3 cycles.
Si les saignements irréguliers persistent ou surviennent après des cycles réguliers, une recherche étiologique non hormonale doit alors être effectuée; des examens diagnostiques appropriés doivent être pratiqués afin d'exclure une tumeur maligne ou une grossesse. Ces examens peuvent comporter un curetage.
Chez certaines femmes, les hémorragies de privation peuvent ne pas survenir au cours de l'intervalle libre. Si la contraception orale a été suivie telle que décrite dans la rubrique Posologie et mode d'administration, il est peu probable que la femme soit enceinte. Cependant, si la contraception orale n'a pas été suivie correctement avant l'absence de la première hémorragie de privation ou si deux hémorragies de privation successives ne se produisent pas, il convient de s'assurer de l'absence de grossesse avant de poursuivre cette contraception.
Excipients à effet notoire
Ce médicament contient du saccharose. Les patients présentant une intolérance au fructose, un syndrome de malabsorption du glucose et du galactose ou un déficit en sucrase/isomaltase (maladies héréditaires rares) ne doivent pas prendre ce médicament.
Ce médicament contient du lactose. Les patients présentant une intolérance au galactose, un déficit total en lactase ou un syndrome de malabsorption du glucose et du galactose (maladies héréditaires rares) ne doivent pas prendre ce médicament.
Précautions d'emploi
Obésité (IMC > = 30 kg/m²)
Traumatisme majeur
Immobilisation temporaire
Antécédent familial thrombo-embolique
Cancer
Lupus érythémateux disséminé
Syndrome hémolytico-urémique
Maladie inflammatoire chronique de l'intestin
Maladie de Crohn
Rectocolite hémorragique
Drépanocytose
Femme de plus de 35 ans
Post-partum jusqu'au retour de couches
Tabagisme
Hypertension artérielle
Migraine
Diabète
Valvulopathie cardiaque
Fibrillation auriculaire
Dyslipoprotéinémie
Douleur de l'hypochondre droit
Augmentation du volume du foie
Hémorragie intra-abdominale
Hypertriglycéridémie
Antécédent familial d'hypertriglycéridémie
Hypertension artérielle non contrôlée
Angio-oedème héréditaire
Angioedème
Anomalie hépatique (tests fonctionnels)
Antécédent d'ictère cholestatique de la grossesse
Antécédent de prurit gravidique
Ictère cholestatique
Prurit de cholestase
Lithiase biliaire
Porphyrie
Chorée de Sydenham
Herpès gravidique
Otosclérose
Dépression
Epilepsie
Changement d'humeur
Symptôme dépressif
Antécédent de chloasma gravidique
Prédisposition au chloasma
Hyperprolactinémie
Surveillance pression artérielle
Troubles gastro-intestinaux
Spotting
Absence d'hémorragie de privation
Vomissement
Diarrhée
Interaction avec d'autre médicaments
Les interactions entre les contraceptifs estroprogestatifs et d'autres substances peuvent conduire à une augmentation ou une diminution des concentrations plasmatiques d'estroprogestatifs.
La diminution des concentrations plasmatiques d'estroprogestatifs peut provoquer une augmentation de l'incidence des saignements intermenstruels et éventuellement réduire l'efficacité du contraceptif estroprogestatif.
Associations contre-indiquées
+ Millepertuis
Diminution des concentrations plasmatiques du contraceptif hormonal, en raison de l'effet inducteur enzymatique du millepertuis, avec risque de baisse d'efficacité voire d'annulation de l'effet dont les conséquences peuvent être éventuellement graves (survenue d'une grossesse).
+ Ombitasvir/Paritaprévir/Ritonavir, Dasabuvir (avec ou sans ribavirine), Glécaprévir/Pibrentasvir et Sofosbuvir/velpatasvir/voxilaprévir
Augmentation de l'hépatotoxicité.
Interactions pharmacodynamiques
L'utilisation concomitante de médicaments contenant l'association ombitasvir/paritaprévir/ritonavir, le dasabuvir, avec ou sans ribavirine, le glécaprévir/pibrentasvir et le sofosbuvir/velpatasvir/voxilaprévir, peut augmenter le risque d'élévation des ALAT (voir rubriques Contre-indications et Mises en garde et précautions d'emploi). Dès lors, les utilisatrices de LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN doivent changer de méthode de contraception (par exemple contraceptif à base de progestatif seul ou méthodes non‑hormonales) avant de débuter un traitement avec ces médicaments. LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN peut être réinstauré 2 semaines après la fin du traitement avec ces médicaments.
Associations déconseillées
+ Inducteurs enzymatiques
(Par exemple apalutamide, carbamazépine, dabrafénib, éfavirenz, enzalutamide, eslicarbazépine, fosphénytoïne, létermovir, lorlatinib, lumacaftor, névirapine, oxcarbazépine, phénobarbital, phénytoïne, pitolisant, primidone, rifabutine, rifampicine)Diminution de l'efficacité contraceptive, par augmentation du métabolisme hépatique du contraceptif hormonal par l'inducteur.
Utiliser une méthode additionnelle de type mécanique (préservatif) pendant la durée de l'association, et un cycle suivant l'arrêt de l'inducteur.
+ Inhibiteurs de protéases boostés par ritonavir
(Par exemple atazanavir, darunavir, fosamprénavir, lopinavir, ritonavir, saquinavir, tipranavir)
Risque de diminution de l'efficacité contraceptive par diminution des concentrations en contraceptif hormonal due à l'augmentation de son métabolisme hépatique par le ritonavir.
Utiliser une méthode additionnelle de type mécanique (préservatif) pendant la durée de l'association, et un cycle suivant l'arrêt du ritonavir.
+ Lamotrigine (voir aussi ci-dessous Associations nécessitant des précautions d'emploi)
Diminution des concentrations et de l'efficacité de la lamotrigine par augmentation de son métabolisme hépatique.
Eviter de mettre en route une contraception orale pendant la période d'ajustement posologique de la lamotrigine.
+ Modafinil
Risque de diminution de l'efficacité contraceptive, pendant le traitement et un cycle après l'arrêt du traitement par le modafinil, en raison de son potentiel inducteur enzymatique.
Utiliser une méthode additionnelle de type mécanique (préservatif) pendant la durée de l'association, et un cycle suivant l'arrêt du modafinil.
+ Pérampanel
Pour des doses de pérampanel ≥ 12 mg/j : risque de diminution de l'efficacité contraceptive.
Utiliser de préférence une autre méthode contraceptive, en particulier de type mécanique.
+ Topiramate
Pour des doses de topiramate ≥ 200 mg/jour : risque de diminution de l'efficacité contraceptive par diminution des concentrations en estrogène.
Si l'association s'avère nécessaire, utiliser une méthode additionnelle de type mécanique pendant la durée de l'association, et un cycle suivant l'arrêt du topiramate.
+ Ulipristal
Dans l'indication contraception d'urgence
Antagonisme des effets de l'ulipristal en cas de reprise d'un contraceptif hormonal moins de 5 jours après la prise de la contraception d'urgence.
Dans le cas où la (re)prise d'une contraception hormonale est envisagée, utiliser une contraception additionnelle de type mécanique pendant les 12 jours qui suivent la (dernière) prise de l'ulipristal (au cas où il y en aurait eu plus d'une).
Dans l'indication fibrome
Antagonisme réciproque des effets de l'ulipristal et du progestatif, avec risque d'inefficacité.
Dans le cas où la (re)prise d'une contraception hormonale est envisagée, utiliser une contraception de type mécanique pendant les 7 premiers jours de la contraception hormonale.
+ Vémurafénib
Risque de diminution des concentrations des estroprogestatifs, avec pour conséquence un risque d'inefficacité.
Associations faisant l'objet de précautions d'emploi
+ Aprépitant
Diminution de l'efficacité contraceptive par augmentation du métabolisme hépatique du contraceptif hormonal par l'aprépitant.
Utiliser une méthode additionnelle de type mécanique (préservatif) pendant la durée de l'association, et un cycle suivant l'arrêt de l'aprépitant.
+ Bosentan
Diminution de l'efficacité contraceptive par augmentation du métabolisme hépatique du contraceptif hormonal par le bosentan.
Utiliser une méthode additionnelle de type mécanique (préservatif) pendant la durée de l'association, et un cycle suivant l'arrêt du bosentan.
+ Elvitégravir
Diminution de l'efficacité contraceptive par augmentation du métabolisme hépatique du contraceptif hormonal par l'elvitégravir.
Utiliser une méthode additionnelle de type mécanique (préservatif) pendant la durée de l'association, et un cycle suivant l'arrêt de l'elvitégravir.
+ Griséofulvine
Diminution de l'efficacité contraceptive par augmentation du métabolisme hépatique du contraceptif hormonal par la griséofulvine.
Utiliser une méthode additionnelle de type mécanique (préservatif) pendant la durée de l'association, et un cycle suivant l'arrêt de la griséofulvine.
+ Lamotrigine
Diminution des concentrations et de l'efficacité de la lamotrigine par augmentation de son métabolisme hépatique.
Surveillance clinique et adaptation de la posologie de la lamotrigine lors de la mise en route d'une contraception orale et après son arrêt.
+ Rufinamide
Diminution de l'efficacité contraceptive par augmentation du métabolisme hépatique du contraceptif hormonal par le rufinamide.
Utiliser une méthode additionnelle de type mécanique (préservatif) pendant la durée de l'association, et un cycle suivant l'arrêt du rufinamide.
Informations complémentaires pour LEVONO/ETHINY BIOGARAN 30microgrammes/150microgr cp
Documents associés
ADEPAL_MINIDRIL_TRINORDIOL_26062019_AVIS_CT16961
Télécharger le documentADEPAL-MINIDRIL-TRINORDIOL_12062019_TRANSCRIPTION_CT16961
Télécharger le documentQ/R « Vous et votre traitement en cas de vague de chaleur »
Télécharger le documentMise au point sur le bon usage des médicaments en cas de vague de chaleur
Télécharger le documentConservation des médicaments en cas de vague de chaleur
Télécharger le documentevolution de l'utilisation en France des conatrceptifs oraux combinés COC de janvier 2013 à décembre 2015
Télécharger le documentImpact de la modification récente des méthodes de contraception en France sur la survenue d'embolies pulmonaires chez les femmes de 15 à 49 ans
Télécharger le documentEvolution de l 'utilisation en France des Contraceptifs Oraux Combinés (COC) et autres contraceptifs de janvier 2013 à avril 2014
Télécharger le documentContraceptifs hormonaux combinés : rester conscient des différences entre les spécialités face au risque thromboembolique, de l'importance des facteurs de risque individuels, et être attentif aux manifestations cliniques
Télécharger le documentListe des spécialités concernées par la réévaluation européenne des contraceptifs hormonaux combinés
Télécharger le documentDOCUMENT D'AIDE A LA PRESCRIPTION CONTRACEPTIFS HORMONAUX COMBINÉS
Télécharger le documentPoint sur l'évolution de l'utilisation des contraceptifs depuis 1 an et sur les actions de sécurisation mises en place
Télécharger le documentVOUS et ... Vos contraceptifs oestroprogestatifs
Télécharger le documentContraceptifs hormonaux combinés (pilules, anneau vaginal et patch) : Position finale du Comité des médicaments à usage humain (CHMP) - Point d'information
Télécharger le documentMédicaments contenant le facteur VIII octocog alpha, médicaments contenant de l'hydroxyéthylamidon, médicaments contenant du valproate, les contraceptifs hormonaux combinés, cabazitaxel (Jevatana) – Retour d'information sur le PRAC
Télécharger le documentL'ANSM publie un nouveau point sur l'évolution de l'utilisation des contraceptifs sur 9 mois
Télécharger le documentRetour d'information sur le PRAC
Télécharger le documentEvolution de l'utilisation en France des Contraceptifs Oraux Combinés (COC) et autres contraceptifs de décembre 2012 à mai 2013
Télécharger le documentPoint presse « COC » du 26 juin 2013
Télécharger le documentQuestions – Réponses pilule contraceptive
Télécharger le documentPlan d'actions sur les contraceptifs oraux combinés - point de situation à juin 2013 - Communiqué
Télécharger le documentNouveau point sur l'évolution récente de l'utilisation des contraceptifs en France - Communiqué
Télécharger le documentL'ANSM publie un nouveau point sur l'évolution de l'utilisation des pilules estroprogestatives - Communiqué
Télécharger le documentPoint d'information sur les dossiers discutés en commission de suivi du rapport bénéfice/risque des produits de santé - Séance du mardi 19 mars 2013
Télécharger le documentRisque thromboembolique veineux attribuable aux contraceptifs oraux combinés (COC) et évolution de leur utilisation : résultats des études de l'ANSM
Télécharger le documentL'Agence européenne ouvre de nouveaux chantiers de réévaluation du bénéfice/risque de médicaments
Télécharger le documentActualisation des données sur les contraceptifs oraux combinés (COC)
Télécharger le documentPilules de 3ème et 4ème générations : COMMUNIQUE DE PRESSE
Télécharger le documentContraceptifs oraux estroprogestatifs : préférez les « pilules » de 1re ou 2e génération - BON USAGE DU MÉDICAMENT
Télécharger le documentCOC et risque de thrombose veineuse
Télécharger le documentCONTRACEPTIFS ORAUX COMMERCIALISES EN FRANCE AU 1ER SEPTEMBRE 2012
Télécharger le documentContraceptifs oraux combinés1 et risque de thrombose veineuse : prescription des pilules de 2e génération contenant du lévonorgestrel en première intention
Télécharger le documentLes contraceptifs oraux combinés (appelés le plus souvent « pilules »). Questions/Réponses
Télécharger le documentContraceptifs oraux estroprogestatifs et risque de thrombose veineuse - Point d information
Télécharger le documentCLASSIFICATION DES CONTRACEPTIFS ORAUX
Télécharger le documentExcipients
Noyau : Lactose monohydraté, Amidon de maïs, Povidone, Magnésium stéarate, Enrobage : Povidone, Talc, Saccharose, Calcium carbonate, Macrogol 6000, Cire E
Exploitant / Distributeur
BIOGARAN
15 boulevard CHARLES DE GAULLE
92707
COLOMBES CEDEX
Code UCD7 : 9406152
Code UCD13 : 3400894061526
Code CIS : 62351344
T2A médicament : Non
Laboratoire titulaire AMM : BIOGARAN
Laboratoire exploitant : BIOGARAN
Prix vente TTC : 3.76€
Taux de TVA : 2.1%
TFR (Tarif Forfaitaire de Responsabilité) : Oui
Base de remboursement : 3.76€
Taux SS : 65%
Agréments collectivités : Oui
Code acte pharmacie : PH7
Date AMM : 13/10/2014
Rectificatif AMM : 31/12/2020
Marque : LEVONORGESTREL ETHINYLESTRADIOL
Gamme : Sans gamme
Code GTIN13 : 3400928023476
Référence LPPR : Aucune
Equivalences strictes
LEVONORGESTREL/ETHINYLESTRADIOL BIOGARAN 150 microgrammes/30 microgrammes, comprimé enrobé, boîte de 1 plaquette de 21
LUDEAL Gé 0,15 mg/0,03 mg Comprimé boîte de 1 plaquette de 21
LUDEAL Gé 0,15 mg/0,03 mg 30microgrammes/150microgr Comprimé boîte de 3 plaquettes de 21
MINIDRIL, comprimé enrobé, boîte de 1 plaquette de 21